인류의 건강과 생명공학 발전을 위해 봉사하는 기업 드림셀
We Serving the Health and Biotechnology of Humanity
We Serving the Health and Biotechnology of Humanity
안녕하세요 프로메가(Promega) 공식대리점 드림셀 입니다.
프로메가에서 Small Molecule Drug Discovery 두번째 이야기 :
암 연구의 혁신 - NCI-60 패널의 역할대한 새로운 뉴스레터를 전해드립니다!
궁금하신점이 있다면 아래로 연락 부탁드립니다
Tel | 02-2292-8870 E-Mail | dreamcell@dreamcell.co.kr
Promega의 Metabolism 시리즈 만나보기
첫번째이야기 보러가기
NCI-60의 개발
초기 단계의 화학 요법 약물은 주로 주요 제약회사 연구소에서 개발되었지만, 많은 중요한 치료제는 NCI가 후원하는 임상 시험을 통해 개발되었습니다. 1980년대 후반, NCI는 암 치료를 위한 신약 개발 과정을 혁신적으로 개선하기 위해 NCI-60 패널을 개발했습니다(2). 이 패널 개발 이전에는 암 치료의 발전이 느려 매년 한두 개의 새로운 화합물만 승인되었기 때문에, NCI-60 패널의 주요 목표는 다양한 암에 대해 특정 활성을 가진 화합물을 식별하고, 감수성과 저항성의 광범위한 패턴을 밝히는 것이었습니다.
NCI의 약물 스크리닝 발전 과정
1955년 설립된 NCI 스크리닝 프로그램은 주로 마우스 백혈병 모델에 의존해 왔으며, 1975년부터 1985년까지 P388 마우스 백혈병 모델이 1차 스크리닝 역할을 했습니다(3). 이 모델에서 인간의 백혈병과 림프종에 대한 치료 결과는 개선되었지만, 대부분의 인간 고형 종양에 대한 치료 결과는 좋지 않았습니다. 이에 NCI는 1976년에 주요 고형 종양 모델을 포함하는 새로운 종양 패널을 출시하여 2차 스크리닝에 사용했습니다(4). 그러나 전임상 스크리닝 결과가 임상에 잘 반영되지 않았기 때문에 보다 대표적인 모델이 필요했습니다.
1985년 인간 고형 종양의 분자적 다양성에 대한 인식이 높아지면서 NCI-60 패널 개발이 시작되었고, 1990년에 NCI-60 패널이 공식적으로 구현되면서 스크리닝 접근법이 '화합물 중심'에서 '질병 중심'으로 전환되었습니다. 초기에는 96 well plate를 사용한 high throughput 스크리닝 방법을 최적화하는 단계를 진행했으며, 대규모 세포주 배양, 자동화된 시약 처리, 소형화된 미세 배양 분석이 가능한 방법을 구현하고자 했습니다. 처음에는 MTT assay를 사용하여 cell viability를 측정했지만 여러 분석 조건에 영향을 받는 문제가 불거졌고, 이를 대체할 방법으로 SRB (Sulforhodamine B) assay를 채택하여 더 높은 민감도와 안정성을 제공할 수 있었습니다(5, 6).
NCI는 1990년대 초부터 최근까지 스크리닝 과정 중 약물에 의한 세포 독성을 측정하기 위한 endpoint 분석에 SRB assay를 사용해 왔습니다. 과학의 발전에 따라 cell viability와 cytotoxicity를 정량화하는 방법이 더욱 최적화되었고, 최근에는 Promega의 CellTiter-Glo® Assay를 endpoint 분석에 채택하여 더욱 정확한 결과를 제공하고 있습니다.
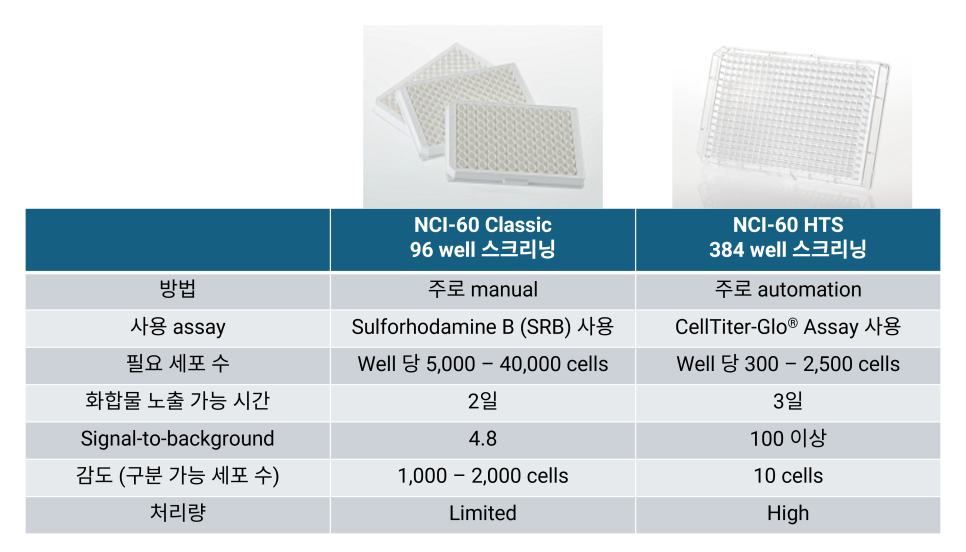
이전의 NCI-60 classic 96 well 스크리닝 방법과 발전된 NCI-60 HTS 384 well 스크리닝 방법 비교
SRB와 CellTiter-Glo® assay는 모두 cell viability와 cytotoxicity를 평가하는 데 널리 사용됩니다. SRB 분석은 culture plate에 고정된 세포의 단백질 성분에 결합하는 SRB dye를 사용하여 세포 밀도에 비례한 흡광 기반의 측정값을 제공합니다(7). 그러나 SRB dye를 이용한 방법은 살아있는 세포와 죽은 세포를 구분할 수 없고, 세포의 분포 정도나 washing 과정에 영향을 받을 수 있습니다. 반면, CellTiter-Glo® assay는 대사적으로 활성 상태의 세포 marker인 세포 내 ATP 양을 측정합니다. 생성된 발광 값은 넓은 dynamic range 내에서 측정되며 세포 내 ATP의 양에 비례하는 생존 가능한 세포 수를 정확히 반영합니다.
새로 구현된 CellTiter-Glo® assay의 workflow는 기존의 SRB assay의 한계를 극복했습니다. 예를 들어, CellTiter-Glo® assay를 통해 세포 내 ATP를 측정하여 살아있는 세포를 직접 측정할 수 있으며, 발광 signal은 세포 수에 상관없이 고밀도 및 저밀도로 배양한 세포 모두에서 더 높은 감도로 안정적인 결과를 보여줍니다. CellTiter-Glo® assay는 SRB assay로는 측정할 수 없는 non-adherent 세포의 cell viability와 cytotoxicity를 측정할 수 있어 사용자의 선택지를 더욱 넓혀줍니다.
또한 CellTiter-Glo® assay는 high throughput screening (HTS)에 적합합니다. SRB assay와 달리, CellTiter-Glo® assay는 세포에 시약을 추가하고 짧은 처리 시간 후 발광 깂을 측정하는 간단한 단계를 거칩니다. 높은 감도와 signal-to-background ratio 덕분에 적은 수의 세포와 샘플로도 측정이 가능해, NCI는 384-well plate를 채택하여 처리량을 늘릴 수 있었습니다. 또한, CellTiter-Glo® assay의 발광 signal은 반감기가 5시간 이상으로 안정적이기 때문에 injector 없이 여러 plate를 일괄 처리할 수 있고 실험 단계가 간단해 HTS 프로세스의 유연성과 정확성을 높입니다.
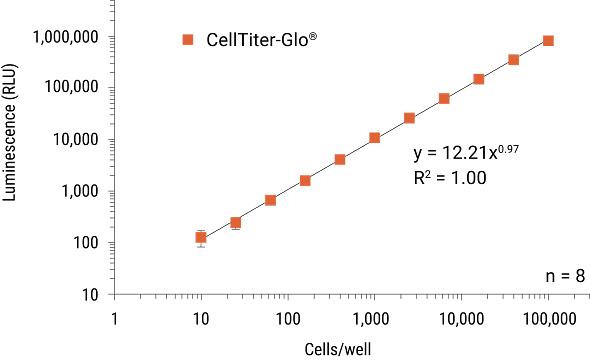
CellTiter-Glo® Cell Viability Assay는 10개의 세포까지 측정할 수 있는
높은 감도를 가지며, 최대 5-log의 linear range를 제공합니다.
NCI-60 패널은 화학 요법 약물, 천연물 등 100,000개 이상의 화합물을 스크리닝하여 전 세계 연구자들에게 중요한 데이터를 제공해 왔습니다. 이 데이터는 전 세계 연구자들에게 공개되어 활용되고 있습니다.
NCI-60은 암 연구와 신약 개발에 지속적으로 활용되고 있으며, 패널의 분자 특성을 업데이트하고 확장하려는 노력으로 그 유용성이 더욱 높아질 것입니다. 최근 도입된 CellTiter-Glo® assay는 스크리닝의 효율성, 신뢰성, 민감도를 향상시켜 고품질 데이터를 제공합니다. 암 연구가 개인화된 표적 치료로 발전함에 따라 NCI-60 패널은 중요한 자원으로 남아 있습니다. NCI-60은 새로운 암 치료법을 식별하고 암의 분자적 환경을 탐구하는 데 큰 기여를 하고 있습니다.